马上注册,结交更多好友,享用更多功能,让你轻松玩转社区。
您需要 登录 才可以下载或查看,没有账号?立即注册

x
本帖最后由 小杨 于 2022-8-18 17:43 编辑
/ k$ m4 p0 ]& [. l
5 `. g0 f+ U, `7 W& m- J
) }: s) o! _0 M* s1 r作者:闵 ) o2 j6 \* G, K5 r/ S) K
脑转移一直是肿瘤患者最头疼的问题之一,毕竟脑转移会很明显影响病人的生存期,并且可能造成头晕、头疼,甚至神志不清等影响,极大降低病人的生存质量。
: b! ]( X2 j, |; t4 [8 {出于对脑转的恐惧,很多病友会到处寻找“灵丹妙药”,学习网上经验,在网络众多脑转移治疗经验中有关“因为血脑屏障,所以化疗药物不入脑”的观点传播非常广泛,以此延伸出“免疫治疗也不入脑”,进而演变成“只有靶向药入脑”甚至只有XX靶向药才入脑,那么事实真的如此吗? 5 }8 m7 y" t2 W
本文从脑转移治疗方式以及临床研究数据等方面,聊一聊是不是真的只有靶向药才能救脑转。
, w" i- O0 g; N: Z+ N7 _脑转治疗方式 ' W* f7 z2 d3 i- ?9 p
脑转移在很多癌种中都容易出现,比如肺癌、乳腺癌等等,脑转移的治疗方式也有很多种,大体上可以分为局部治疗与全身性治疗两大类。局部治疗主要包括手术与放疗两种方式,这里不做过多讨论,本文重点和各位聊一聊脑转移的药物全身性治疗。
$ L1 F5 S2 D* N7 X# y无论是化疗、靶向,还是免疫治疗,都会通过体循环达到全身各个部位,故而称为全身性治疗。由于血脑屏障、脑转移后形成的血瘤屏障,以及药物排出泵等存在可能影响药物在脑部的血药浓度,但并不意味着全身性治疗完全无法越过屏障达到治疗目的。 / t4 g3 ~- _0 n0 S7 e/ `
《肺癌脑转移中国治疗指南(2021版)》及《中国结直肠癌脑转移多学科综合治疗专家共识(2020版)》中列举的内科治疗方式恰恰仍旧是化疗、靶向、抗血管生成药物以及免疫治疗这些手段。即便是药物相对较窄的肠癌脑转移治疗,专家组认为虽然有血脑屏障的存在,使得化疗疗效欠佳,但对于经历过手术及放疗的患者,在全身得以控制的情况下,联合化疗仍可增加疗效。 + H+ v; l7 Y& U% Y" k, \
例如在接受过手术及放疗的结直肠癌脑转移患者,行XELOX(卡培他滨+奥沙利铂)/FOLFIRI(5-氟尿嘧啶+亚叶酸钙+伊立替康)联合贝伐单抗或长期口服S-1(替吉奥)维持治疗,在一定程度上可以起到控制病情发展的作用。 ) p- Y" S1 y& v, M z9 z6 Z0 e2 M P
各类药物颅内疗效 & T3 B4 \9 |8 n8 @4 A( _
前面说了很多都是指南与专家共识的指导意见,各位可能觉得都是规范太空洞,所以我找了一些肠癌、肺癌以及其他癌种使用化疗、抗血管生成药治疗脑转移的案例及临床数据,供各位切实了解。 * m( V. P, K7 X9 E, g9 U: y
化疗
9 G9 @( P: U, Z5 p# N0 }+ N7 |) w1、2014年[1]日本报道一例62岁男性患者,肝脏有10余处转移,脑部两处转移,接受了脑转移切除手术,还有一处脑转移病灶,后接受XELOX(卡培他滨+奥沙利铂)+贝伐治疗,4个周期后复查,脑转移病灶缩小。2017年[2]日本一例案例报道60岁的女性VI期肠癌患者在放化疗后原发灶及肝脏转移均消失,但治疗期间出现脑转移,行放疗及手术,后长期服用S-1(替吉奥),6年未见复发。
% w. q, ?7 R4 c7 Z) {8 q4 v2、2011年发表的GFPC 07-01研究[3]纳入42名无症状的脑转移NSCLC患者,接受培美曲塞+顺铂的治疗方案,结果如下表,颅内RR为41.9%,颅外(即全身)ORR为34.9%。很明显培美曲塞+顺铂的方案可以入脑,且颅内有效率并不比其他部位有效率低。
; I9 ?" t$ S1 S1 k6 Q3、2015年的一项回顾性研究[4]纳入了776例脑转移NSCLC患者,分为化疗组,化疗+贝伐组,靶向药组以及支持治疗组,研究分析了不同细胞毒性药物对于脑转移患者的有效率(培美曲塞与紫衫类药物),培美曲塞组整体ORR为32.7%,颅内ORR为41.8%,而紫衫类组的整体ORR为26.5%,颅内ORR为30.2%。
7 P' V) T) |6 n; [( x4、2002年的一项II期临床研究[5]一线联合长春瑞滨+吉西他滨+顺铂治疗脑转移的NSCLC患者,结果表明20名可测量患者的颅内ORR为45%(3例CR,6例PR),另外颅内病灶有效的病人在其他部位转移灶也发现有效。 : h, M* c. G* s; T% @2 R3 x f
5、替莫唑胺本身是脑胶质瘤的常用药物,能较好的透过血脑屏障,因此很早开始就有一些研究尝试应用于其他脑转移瘤的治疗,在2002年一项II期研究[6]纳入了38例既往接受过脑部放疗或者化疗的脑转移患者接受替莫唑胺治疗,结果有效率仅8%,DCR为40%,总体样本量偏小。
9 F& ]+ Q3 o' c& n抗血管生成药- ]$ r3 v- ?% K* z5 |8 ^. d
. p8 M4 x' T) K7 S Q4 gAlter303研究[7]是一项评估安罗替尼用于既往至少接受过二线治疗的中晚期NSCLC患者的研究,其中有97名患者入组时已发生脑转移。结果表明,对于有脑转的病人,安罗替尼的ORR为14.3%,并且与安慰剂对比,安罗替尼延长了PFS与OS(4.17个月,8.57个月)。 ' b; \5 \0 v; o- h% K5 n
2021年发表了一篇回顾性的研究[8]纳入88例脑转移的肾癌患者,其中大部分既往接受过其他全身性治疗,队列A纳入33例,均为脑转移但并未联合其他局部治疗,接受卡博替尼治疗的颅内ORR为55%(3例CR,14例PR),颅外ORR为48%,OS为15.0个月。 5 r8 G# f% e/ \5 a7 K9 H" g6 m" @
免疫治疗 $ E( v8 t% [: t4 c9 R V0 q! }
K药
2 V2 [- g. H0 u一项前瞻性的双臂II期研究[9]评估K药治疗至少有一个大于5mm且小于20mm的脑转移病灶的NSCLC或黑色素瘤患者,共纳入36例可评估患者患者。NSCLC组18例患者,有效率33.3%,有4个病例达到颅内CR。
, Q; H9 G6 z, _$ L9 jO药 7 J) K& P$ \1 Z' }; V$ h" o5 U1 b- c9 A
Lung Cancer上发表了一项O药治疗脑转移NSCLC患者的真实世界疗效研究[10],共纳入1588例患者,其中有409例患者在一开始已经发生脑转移,这部分患者中有29%接受过激素治疗,18%接受过激素同步放疗,59%接受过脑部放疗,在这些治疗手段失败后开始接受O药治疗。
. d( }! f( ~4 l9 o6 X结果显示,脑转移患者中ORR位17%,DCR率为39%,其中有4名患者颅内CR,有效率与总体人群有效率接近,脑转移患者PFS为3个月,OS为8.6个月,1年生存率为20%,需要注意的是这部分脑转患者已经是接受过其他治疗并且失败进展之后的。
- U ]' r1 g- K5 P; s; [靶向治疗
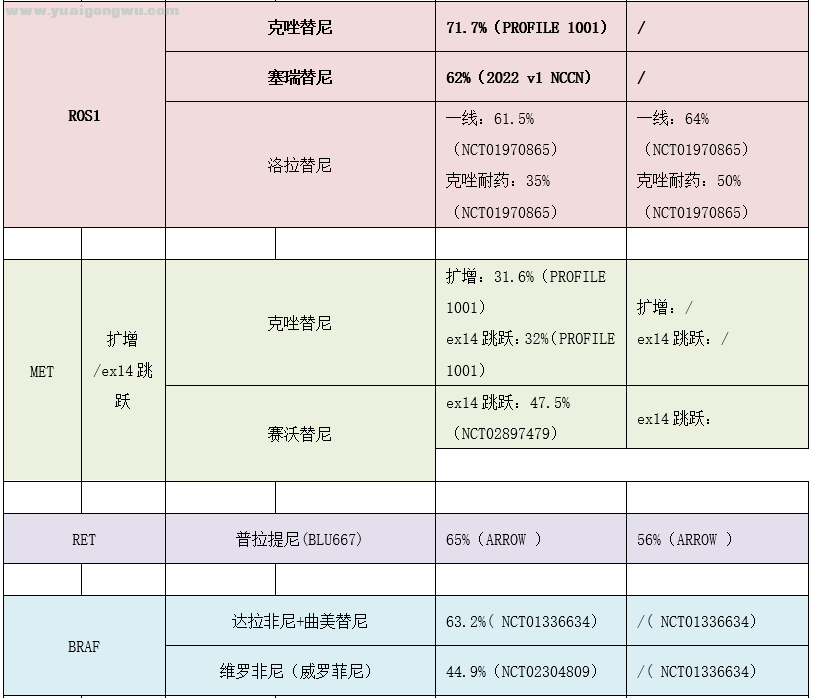
1 h8 `* a) u, h几乎各个靶点对应的靶向药的临床研究都有关于脑转移治疗的评估,故不一一介绍,汇总如下:
7 N9 M& c7 b+ o2 ~' e, s
$ E' e" S2 D! M8 X8 y. J# p
 % W& v1 J( }- {- W/ |! g( ^# D* ~* D, I# d
% W& v1 J( }- {- W/ |! g( ^# D* ~* D, I# d
总结 ' O3 o4 G: J- j l- A* f- }
脑转移在肺癌、乳腺癌以及肠癌等多种癌种中会出现,极大影响病人的生存质量及生存期,一直以来对于脑转移的治疗都是个难题。 9 f# `" ?6 `* x, T8 y) R9 T# a$ v
血脑屏障的存在确实在一定程度上阻碍了脑内的血药浓度,但并非如网上所说“只有XX靶向药才能入脑”,根据以上资料可以看到,指南与专家共识并未完全放弃化疗、抗血管生成药以及免疫治疗,转而完全依赖靶向。 5 S! I1 f0 W5 G a! z! V: q
化疗并非完全不入脑,相反,根据大量研究数据表明,诸如培美曲塞、紫衫类、吉西他滨、长春瑞滨、卡培他滨以及奥沙利铂等常用化疗药非但对颅内病灶有效,而且与颅外有效率相差无几;
9 V- d1 c3 N9 C' d- z) i抗血管生成药种类繁多,大多可用于多种癌种,且无需基因突变,大分子单抗如贝伐单抗与化疗联用可增加颅内控制率,小分子抑制剂如安罗替尼、卡博替尼等单独使用也有机会对颅内病灶有效;
% h8 R( \7 F* B免疫治疗是目前较为新型的治疗方式,也有一定研究表明可能对颅内病灶有效。
$ @& }3 }2 k; L8 u* g靶向药虽然相对有很好的颅内治疗数据,但有一点往往被忽视,即使用靶向药的先决条件是具有相应的靶向基因突变,而非所有脑转患者使用都有效;另外需要注意的是,并非某个特定靶向药才入脑,而是几乎所有靶向药都可以。
, y1 z% V! J# l$ T诚然,化疗及抗血管生成药等全身性治疗的颅内有效率不如靶向药,但毕竟它们适用于更多人群,并不要求必须有特定突变才有效,甚至靶向药失败后也有可能有效,因此希望各位能够正确认识全身性治疗对于各个部位病灶的治疗效用,不要再被谣言蒙蔽,执着于迷信盲试靶向。
! T; _5 e( f" f2 F' {' I9 D( v2 }往期回顾丨闵的其他精彩文章 z# V3 h' D! m+ D" b, m3 @: J
( B8 O7 y& i% l/ T4 P" p参考文献 [1] Yoshida Y, Hoshino S, Aisu N, et al. Efficacy of XELOX plus bevacizumab in brain metastasis from rectal cancer[J]. Case Reports in Oncology, 2014, 7(1): 117-121. [2] Ogawa S, Fujishiro H, Fujiwara A, et al. A case of long-term survival in stage IV squamous cell carcinoma of the anal canal with multidisciplinary treatment[J]. Nihon Shokakibyo Gakkai Zasshi= The Japanese Journal of Gastro-enterology, 2017, 114(11): 1987-1995. [3] Barlesi F, Gervais R, Lena H, et al. Pemetrexed and cisplatin as first-line chemotherapy for advanced non-small-cell lung cancer (NSCLC) with asymptomatic inoperable brain metastases: a multicenter phase II trial (GFPC 07-01)[J]. Annals of oncology, 2011, 22(11): 2466-2470. [4] Tang N, Guo J, Zhang Q, et al. Greater efficacy of chemotherapy plus bevacizumab compared to chemo-and targeted therapy alone on non-small cell lung cancer patients with brain metastasis[J]. Oncotarget, 2016, 7(3): 3635. [5] Bernardo G, Cuzzoni Q, Strada M R, et al. First-line chemotherapy with vinorelbine, gemcitabine, and carboplatin in the treatment of brain metastases from non-small-cell lung cancer: a phase II study[J]. Cancer investigation, 2002, 20(3): 293-302. [6] Adonizio C S, Babb J S, Maiale C, et al. Temozolomide in Non—Small-Cell Lung Cancer: Preliminary Results of a Phase II Trial in Previously Treated Patients[J]. Clinical lung cancer, 2002, 3(4): 254-258. [7] Han B, Li K, Wang Q, et al. Effect of Anlotinib as a third-line or further treatment on overall survival of patients with advanced non–small cell Lung Cancer: The ALTER 0303 Phase 3 Randomized Clinical Trial[J]. JAMA oncology, 2018, 4(11): 1569-1575. [8] Hirsch L, Chanza N M, Farah S, et al. Clinical activity and safety of cabozantinib for brain metastases in patients with renal cell carcinoma[J]. JAMA oncology, 2021, 7(12): 1815-1823. [9] Goldberg S B, Gettinger S N, Mahajan A, et al. Pembrolizumab for patients with melanoma or non-small-cell lung cancer and untreated brain metastases: early analysis of a non-randomised, open-label, phase 2 trial[J]. The lancet oncology, 2016, 17(7): 976-983. [10] Gauvain C, Vauléon E, Chouaid C, et al. Intracerebral efficacy and tolerance of nivolumab in non–small-cell lung cancer patients with brain metastases[J]. Lung Cancer, 2018, 116: 62-66. ' y) I6 E. Y: k7 C G) I
1 W6 ^8 w6 O# S
|